ГОСТ 24861-91
(ИСО 7886-84)
Группа P21
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
ШПРИЦЫ ИНЪЕКЦИОННЫЕ ОДНОКРАТНОГО ПРИМЕНЕНИЯ
Sterile hypodermic syringes for single use
ОКП 94 3284
Дата введения 1992-07-01
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. РАЗРАБОТАН И ВНЕСЕН Министерством медицинской промышленности СССР
РАЗРАБОТЧИКИ
Б.П.Пашинин, канд. техн. наук (руководитель темы); Г.А.Матюшин, д-р техн. наук; А.П.Маслюков, канд. хим. наук; Р.И.Перцов; Н.Б.Васильковская; Т.В.Ерофеева; Т.А.Купцова; Г.С.Курдупова
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Комитета стандартизации и метрологии СССР от 27.11.91 N 1814
Настоящий стандарт разработан методом прямого применения стандарта ИСО 7886-84 "Шприцы инъекционные однократного применения" с дополнительными требованиями, отражающими потребности народного хозяйства
3. Срок первой проверки - 1997 г.
Периодичность проверки - 5 лет
4. ВЗАМЕН ГОСТ 24861-81
5. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка | Номер пункта, подпункта, приложения |
ГОСТ 25046-85* | Введение, разд.2 |
ИСО 594-90 | Введение, разд.2; 15 |
________________
* На территории Российской Федерации действует ГОСТ 25046-81, здесь и далее по тексту. - Примечание изготовителя базы данных.
0. ВВЕДЕНИЕ
0. ВВЕДЕНИЕ
Настоящий стандарт распространяется на шприцы, предназначенные для использования в медицинской практике и отвечающие функциональным требованиям к ним. Стандарт допускает некоторые изменения в конструкции и способе упаковывания и стерилизации шприцев индивидуальными изготовителями.
Материалы, идущие на изготовление стерильных шприцев однократного применения, подробно не характеризуются, так как выбор их зависит от конструкции, способа изготовления и стерилизации, применяемых каждым отдельным изготовителем. Материалы должны быть совместимы с вводимыми препаратами, включенными в соответствующие фармакопеи. В противном случае следует привлечь внимание потребителя к исключениям, указанным на потребительской упаковке.
Большинство инъекций готовят на водных средах, при которых не возникает осложнений. Впрыскиваемые вещества не на водной основе приготовляют на растворе типа эфира, или рабочий ингредиент может сам быть жидкостью. В зависимости от продолжительности контакта некоторые из этих жидкостей могут реагировать с элементами шприца. Нельзя указать универсальный способ испытания на несовместимость, но тем не менее, в приложениях Е и F вместе с обычным способом, который может быть использован для определения видимой или функциональной несовместимости шприца и вводимым препаратом, приводится ряд растворителей и других жидкостей, взятых из фармакопеи, представляющих вещества, используемые для инъекций.
Фармацевтическими заводами используются некоторые жидкости - растворители, не вошедшие в фармакопею. Такие растворители должны испытываться изготовителями инъекционных препаратов на возможную несовместимость с материалами, чаще всего применяющимися при изготовлении шприцев. Виды материалов, получивших широкое применение, приводятся для справки в примечании к п.4.2. В тех случаях, когда имеет место несовместимость, на упаковке инъекционного препарата должна быть соответствующая надпись.
Вышеуказанные способы испытания могут рассматриваться только как средства, указывающие на наличие несовместимости. Единственным правильным и решающим испытанием должна быть проверка на несовместимость между конкретным инъекционным препаратом и конкретным шприцем. В настоящее время невозможно провести испытание того или иного инъекционного препарата со всеми имеющимися шприцами в международном масштабе, поэтому рекомендуется всем законодательным органам, органам и организациям по стандартизации, службам фармакопеи и соответствующим торговым ассоциациям рассмотреть эту проблему на национальном уровне и оказать помощь заводам-изготовителям. Испытания на отсутствие пирогенных веществ, сверхдопустимое содержание токсичных веществ и другие химические испытания по экстрактным веществам проводятся в соответствии с разд.6, 7, 9, F.6, F.7, F.9.
Приложения А, В, С, D и F* составляют неотъемлемую часть настоящего стандарта.
________________
* Приложение F отражает потребности народного хозяйства СССР.
В некоторых странах национальная фармакопея и другие нормативные документы юридически взаимосвязаны, и требования этих документов могут иметь приоритет над настоящим стандартом.
Шприцы для подкожных инъекций, указанные в настоящем стандарте, могут применяться с иглами в соответствии с требованиями ГОСТ 25046 (ИСО 7864).
Технические характеристики соединений с 6%-ной конусностью типа Луер даны в соответствии с требованиями ИСО 594.
1. НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ
________________
* См. приложение F.
Настоящий стандарт определяет требования, предъявляемые к стерильным инъекционным шприцам однократного применения.
Примечания:
1. Стерильные инъекционные шприцы однократного применения, указанные в настоящем стандарте, предназначены для использования сразу же после наполнения и не рассчитаны на длительное содержание инъектируемой жидкости или образцов, например, в перфузионных насосах.
2. Стандарт на инсулиновые шприцы находится в стадии разработки.
В СССР требования настоящего стандарта являются обязательными.
2. ССЫЛКИ
ИСО 594. Конические соединения с 6%-ной конусностью типа Луер для шприцев, игл и другого медицинского оборудования.
ГОСТ 25046 (ИСО 7864). Иглы инъекционные однократного применения. Основные размеры. Технические требования. Методы испытаний.
3. НОМЕНКЛАТУРА
Наименования, используемые для обозначения составных частей инъекционных шприцев однократного применения, даны на черт.1.
Черт.1.Схематическое изображение шприца инъекционного однократного применения
Схематическое изображение шприца инъекционного однократного применения
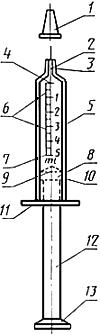
1 - колпачок наконечника*; 2 - отверстие наконечника; 3 - наконечник; 4 - нулевая линия; 5 - цилиндр; 6 - линия градуировки; 7 - номинальная вместимость; 8 - поршень; 9 - линия отсчета; 10 - уплотнитель; 11 - упоры для пальцев; 12 - шток; 13 - упор штока
Черт.1
________________
* В СССР колпачок наконечника допускается не применять.
Примечание. Чертеж иллюстрирует составные части шприца и не является частью спецификации. Конструкция узла шток-поршень может быть как разборной, так и неразборной, а также может иметь более одного уплотнения.
4. МАТЕРИАЛЫ
4.1. Материалы, используемые для изготовления шприцев, должны соответствовать их назначению и быть пригодными для стерилизации*.
________________
* См. приложение F.
4.2. Материалы, используемые для изготовления шприцев, не должны неблагоприятно влиять на их физические или химические характеристики при нормальном использовании инъекционных препаратов (см. разд.0).
Примечание. Для цилиндров стерильных шприцев, используемых для инъекций, широко применяются определенные сорта полипропилена, полистирола и сополимера стирола и акрилонитрила. Для поршня часто применяют высококачественный натуральный каучук, используют также и силиконовый каучук, покрывая поверхность поршня полидиметилсилоксаном. Для уплотнителя двухдетальной конструкции используют полиэтилен высокой плотности в сочетании с полипропиленовым цилиндром, содержащим амидную добавку для лучшего скольжения.
4.3. Материалы, используемые для изготовления шприцев для инъекций, не должны выделять токсичные вещества. Кроме того, шприцы из этих материалов должны отвечать требованиям на отсутствие пирогенных веществ (см. разд.6), сверхдопустимое содержание токсичных веществ (см. разд.7) и требованиям испытаний на допустимое количество экстрагируемых веществ (см. п.9.1).
4.4. Материал, используемый для изготовления цилиндра шприца, должен обладать достаточной прозрачностью для определения дозы.
5. ИЗГОТОВЛЕНИЕ
Шприцы должны изготовляться в соответствии с признанными национальными и международными нормами высококачественного изготовления медицинского оборудования и приборов и не должны иметь дефектов, ухудшающих их внешний вид и надежность при использовании.
6. ОТСУТСТВИЕ ПИРОГЕННЫХ ВЕЩЕСТВ
________________
* См. приложение F.
Шприцы должны удовлетворять требованиям настоящего стандарта при испытаниях на отсутствие пирогенных веществ в соответствии с национальными фармакопеями.
Экстракт, используемый для этого испытания, должен готовиться с соблюдением методики, указанной в п.А.2.
7. ИСПЫТАНИЕ НА СВЕРХДОПУСТИМОЕ СОДЕРЖАНИЕ ТОКСИЧНЫХ ВЕЩЕСТВ
________________
* См. приложение F.
Шприцы должны удовлетворять требованиям настоящего стандарта в части испытаний на сверхдопустимое содержание токсичных веществ, а также требованиям национальной фармакопеи.
Экстракт, используемый в этом испытании, должен готовиться по методу, указанному в п.А.2.
8. ОТСУТСТВИЕ ПОСТОРОННИХ ВЕЩЕСТВ
Поверхность шприца, которая контактирует с инъектируемой жидкостью во время нормального использования, должна быть чистой и не иметь посторонних частиц при осмотре невооруженным глазом.
Примечание. В дальнейшем будет рассмотрен вопрос о разработке стандартных испытаний на определение примесей или посторонних частиц.
9. ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К ЭКСТРАГИРУЕМОМУ ВЕЩЕСТВУ
9.1. Общие положения*
________________
* См. приложение F.
Шприц должен удовлетворять требованиям химических испытаний на экстрагируемое вещество в соответствии с методами, указанными в соответствующих национальных фармакопеях.
9.2. Допустимые содержания кислых и щелочных примесей
рН экстракта должен отвечать требованиям п.А.3;
рН экстракта шприца должен определяться при помощи лабораторного потенциометрического рН-метра, использующего электрод общего назначения. Отклонение значения рН от контрольной жидкости должно быть в пределах одной единицы.
9.3. Пределы содержания экстрагируемых металлов
Экстракт, приготовленный в соответствии с требованиями п.А.3, должен содержать не более 5 мг/кг общего количества свинца, олова, цинка и железа при испытании общепризнанным микроаналитическим методом, например, атомно-абсорбционным методом. Содержание кадмия в экстракте должно быть менее 0,1 мг/кг.
10. СМАЗКА
10.1. Внутренние поверхности шприца, включая поршень, могут быть смазаны смазочным материалом в соответствии с требованиями разд.4.
10.2. Количество смазывающего вещества должно быть минимальным, чтобы не образовывались капли жидкости на внутренней поверхности шприца.
11. РАЗМЕРЫ
Размеры должны соответствовать указанным в табл.1. Однако шприцы могут быть и других размеров. Для этого значения, указанные в табл.1, должны быть экстраполированы или интраполированы.
Таблица 1
Номинальная вместимость шприца, см | Минимальная длина шкалы, мм | Деление шкалы, см | Допуск на любую градуированную вместимость, превышающую половину номинальной, % |
1 | 57 | 0,05 или 0,01 | ±5 |
2 | 27 (26)* | 0,2 или 0,1 | ±5 |
5 | 36 | 0,5 (или 0,2)* | ±4 |
10 | 44 | 1 (или 0,5)* | ±4 |
20 | 52 | 2 (или 1)* | ±4 |
30 | 67 | 2 | ±4 |
50 | 75 | 5 | ±4 |
________________
* В СССР допускается применять значения, указанные в скобках.
12. ВМЕСТИМОСТЬ
12.1. Определение вместимости
Вместимость, соответствующая любому делению шкалы, должна определяться объемом воды при температуре 20 °С, вылившейся из шприца, когда край отсчета поршня пересечет это деление. Вместимость может быть определена путем взвешивания вылившейся жидкости.
12.2. Допуски для градуированной вместимости
Допускаемые пределы для градуированной вместимости должны соответствовать значениям, указанным в табл.1.
13. ГРАДУИРОВАННАЯ ШКАЛА
13.1. Шкала
Шкала должна быть градуирована делениями в соответствии с табл.1 и черт.2. Двойная шкала не допускается, однако, могут использоваться дополнительные деления, если это не противоречит требованиям других стандартов.
Черт.2. Градуировка шкалы шприцев
Градуировка шкалы шприцев
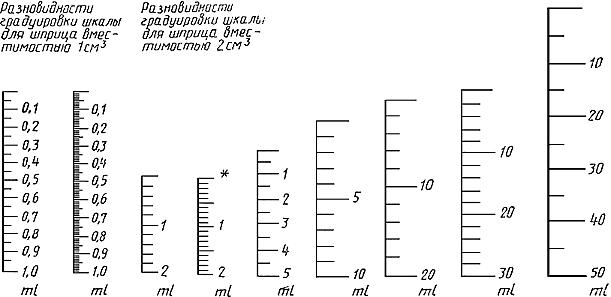
Вертикальная линия шкалы может отсутствовать
Черт.2
________________
* При необходимости могут быть нанесены цифры шкалы 0,5 и 1,5.
Линии градуировки должны быть четкими, заметными и одинаковой толщины. Они должны лежать в плоскости, проходящей строго перпендикулярно оси цилиндра.
Линии градуировки должны быть равно удалены друг от друга вдоль продольной оси между нулевой отметкой и отметкой, обозначающей полную вместимость, в пределах допуска, указанного в табл.1.
При вертикальном положении шприца концы линий градуировки равной длины должны быть строго вертикальны один под другим.
Длина коротких линий деления любой шкалы должна равняться половине длины длинных линий*. И короткие и длинные линии должны быть контрастны между собой.
________________
* В СССР допускается до 01.07.95 отклонение длины малых линий +30%.
13.1*. Цифровые обозначения шкалы
________________
Нумерация соответствует оригиналу. - Примечание изготовителя базы данных.
Линии градуировки, подлежащие маркировке, должны соответствовать указанным на черт.2. Цифровое обозначение шкалы должно наноситься утолщенными линиями и должно быть четким.
При вертикальном положении шприца, когда его конический наконечник расположен сверху, и шкала находится на уровне глаз, цифры на шкале должны быть вертикальными и располагаться так, чтобы пересекаться с продолжением линий, к которым они относятся. Цифры должны находиться рядом с линиями градуировки, к которым они относятся, но не касаться их.
13.3. Общая длина шкалы
Общая длина шкалы должна быть в соответствии с требованиями табл.1.
13.4. Расположение шкалы*
_________________
* См. приложение F.
При нахождении штока в крайнем положении, когда он до упора смещен к отверстию наконечника цилиндра, нулевая отметка шкалы должна совпадать с линией начального отсчета на поршне (п.15.3) в пределах четверти наименьшего деления шкалы.
14. ЦИЛИНДР
_________________
* См. приложение F.
14.1. Размеры
14.1.1. Внутренний диаметр цилиндра должен обеспечивать требования, указанные в табл.1.
14.1.2. Длина цилиндра должна быть такой, чтобы общая вместимость шприца была на 10% больше номинальной величины.
14.2. Упоры для пальцев
Открытый конец цилиндра должен быть снабжен упорами для пальцев, которые должны обеспечивать шприцу устойчивость и удерживать его от скатывания, когда он находится на плоской поверхности шкалой вверх, расположенной под углом 10° к горизонтали.
Примечание. Упоры для пальцев должны быть соответствующего размера, формы и прочности, отвечающих их назначению, и должны позволять прочно удерживать шприц при его применении. Упоры для пальцев не должны иметь заусенцев и острых краев.
15. ШТОК-ПОРШЕНЬ
15.1. Общие положения
Конструкция штока и упора штока шприца должна быть такой, чтобы при удерживании одной рукой шток мог быть утоплен большим пальцем этой же руки. Поршень не должен отделяться от штока при всасывании во время испытания, указанного в приложении С.
15.2. Предпочтительная длина штока
Шток должен быть такого размера, чтобы поршень мог проходить по всей длине цилиндра. При совпадении торца поршня с нулевой отметкой шкалы шток должен выступать из цилиндра на величину, указанную в табл.2.
Таблица 2
Номинальная вместимость шприца, см | Минимальная длина выступания от верха цилиндра до верха стержня штока, мм |
1 | 8,0 |
2 | 9,0 (8,0)* |
5 | 12,5 (9,0)* |
10 | 12,5 (10,0)* |
20 | 12,5 (10,0)* |
30 | 12,5 |
50 | 12,5 |
________________
* В СССР допускается применять значения, указанные в скобках.
Длина выступания штока и форма его упора должны быть такими, чтобы шток легко мог быть выдвинут.
15.3. Линия отсчета
Четко выраженная линия на конце поршня служит линией отсчета для определения вместимости, соответствующей любому делению шкалы шприца. Линия отсчета должна тесно соприкасаться с внутренней поверхностью цилиндра.
15.4. Посадка поршня в цилиндре
Посадка поршня в цилиндре должна быть такой, чтобы поршень плавно скользил по всей градуированной длине цилиндра.
16. НАКОНЕЧНИК
16.1. Коническое соединение
Конический наконечник шприца должен соответствовать требованиям ИСО 594.
16.2. Положение наконечника на конце цилиндра
16.2.1. У шприцев вместимостью 1 и 2 см наконечник должен располагаться по центру, т.е. соосно с цилиндром.
16.2.2. У шприцев вместимостью 5 см и более наконечник может располагаться как по центру, так и эксцентрично.
16.2.3. Если наконечник шприца эксцентричен, он должен располагаться под осью цилиндра, когда лежит на плоской поверхности шкалой вверх; расстояние между осью наконечника и ближайшей точкой внутренней поверхности цилиндра не должно превышать 4,5 мм.
16.3. Отверстие
Наконечник должен иметь центральное отверстие диаметром не менее 1,2 мм.
16.4. Колпачок наконечника
На наконечнике может быть колпачок.
17. РАБОТА ШПРИЦА В СБОРКЕ
17.1. "Мертвое" пространство
Объем жидкости, содержащейся в цилиндре и наконечнике при утопленном до упора поршне, должен быть в соответствии с табл.3 и приложением D.
Таблица 3
см
Номинальная вместимость шприца | Максимальный объем "мертвого" пространства |
1 | 0,07 |
2 | 0,07 |
5 | 0,07 |
10 | 0,10 |
20 | 0,15 |
30 | 0,17 |
50 | 0,20 |
17.2. Испытания на герметичность конического соединения
При испытании, как указано в приложении В, не должно быть утечки в соединении шприц-игла и контрольном коническом соединении. При проверке, указанной в п.С.2 приложения С, не должны образовываться воздушные пузырьки в соединении шприц-игла и в контрольном коническом соединении.
17.3. Испытания на водо- и воздухонепроницаемость поршня
При испытании, как указано в приложении В, не должно быть утечки воды через поршневое уплотнение.
При испытании, как указано в приложении С.1, не должно быть утечки воздуха через поршневое уплотнение и не должно падать показание манометра.
18. УПАКОВКА
18.1. Упаковывание шприца
Каждый шприц должен быть герметически упакован, материал для упаковки не должен оказывать вредного воздействия на содержимое. Материал и конструкция упаковки должны обеспечивать:
а) сохранность стерильности содержимого при хранении в сухих, чистых и хорошо проветриваемых помещениях;
б) минимальный риск загрязнения содержимого при вскрытии и извлечении из упаковки;
в) надежную защиту содержимого при нормальном обращении, перевозке и хранении;
г) возможность обнаружения вскрытия упаковки в том случае, если целостность ее нарушена, а также недопустимость повторной заварки упаковки.
18.2. Внешняя упаковка
Внешняя упаковка должна быть достаточно прочной и надежной и содержать такое количество шприцев, чтобы предохранить содержимое упаковки при транспортировании и хранении.
19. СТЕРИЛЬНОСТЬ
________________
* См. приложение F.
Содержимое упаковки (п.18.1) должно быть стерильным.
Примечание. Государственные органы могут требовать соответствия шприцев требованиям фармакопейных испытаний или другим нормативным документам.
20. МАРКИРОВКА УПАКОВКИ
20.1. Потребительская упаковка*
________________
* См. приложение F.
Потребительская упаковка шприца должна иметь следующую маркировку:
а) описание содержимого;
б) слово "СТЕРИЛЬНО";
в) слова "ДЛЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ" или их заменяющие.
Примечание. Применение термина "выбрасываемый" не допустимо;
г) при необходимости предупреждение о несовместимости с растворителем, например, "Не применять с паральдегидом";
Примечание. Смотри также замечание о совместимости, приведенные в разд.0;
д) наименование и (или) товарный знак предприятия-изготовителя или поставщика;
е) номер партии или дату изготовления.
20.2. Внешняя упаковка*
________________
* См. приложение F.
Внешняя упаковка должна иметь следующую маркировку:
а) описание содержимого;
б) слово "СТЕРИЛЬНО";
в) слова "ДЛЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ" или их заменяющие;
г) указание о проверке целостности каждой упаковки шприца*;
________________
* В СССР указание о проверке целостности упаковки (групповой тары) приводят в Инструкции по эксплуатации.
д) маркировку партии (п.20.1) и дату (месяц и год) стерилизации;
е) наименование и адрес предприятия-изготовителя или поставщика.
ПРИЛОЖЕНИЕ А. ПРИГОТОВЛЕНИЕ ЭКСТРАКТОВ
ПРИЛОЖЕНИЕ А
Обязательное
А.1. Методика приготовления*
________________
* См. приложение F.
Три шприца заполняют в асептических условиях экстракционной жидкостью до номинальной вместимости и в течение 8 ч выдерживают при температуре 37 °С. Затем жидкость сливают в емкость из боросиликатного стекла.
А.2. Экстракт для испытания на пирогенность и сверхдопустимое содержание токсичных веществ
Готовят экстракт, как указано в п.А.1, используя стерильный, не содержащий пирогенных веществ физиологический соляной раствор, имеющий концентрацию 9 г аналитически чистого хлористого натрия на 1 дм свежеприготовленной дистиллированной воды.
А.3. Экстракт и контрольная жидкость для испытания на кислотно-щелочные и экстрагируемые вещества
Готовят экстракт, как указано в п.А.1, используя свежеприготовленную дистиллированную воду в качестве экстракционной жидкости.
Готовят контрольную жидкость, оставив аликвотную часть неиспользованной экстракционной жидкости.
ПРИЛОЖЕНИЕ В (обязательное). ИСПЫТАНИЕ ПОРШНЯ И НАКОНЕЧНИКА ШПРИЦА НА ГЕРМЕТИЧНОСТЬ ПОД ДАВЛЕНИЕМ
ПРИЛОЖЕНИЕ В*
Обязательное
________________
* См. приложение F.
Испытание проводят следующим образом.
В.1. Соединяют наконечник шприца со стальной контрольной втулкой (обе части должны быть сухими). Контрольная втулка должна иметь внутреннюю 6%-ную конусность Луер в соответствии с требованиями ИСО 594. Соединяют части, прикладывая осевое усилие 27,5 Н в течение 5 с и поворачивая их не более чем на 90°, с крутящим моментом, не превышающим 0,1 Н/м.
В.2. Набирают в шприц воды, объем которой превышает градуированную вместимость шприца. Соединение втулки с наконечником должно быть сухим.
В.3. Выпускают воздух.
В.4. Устанавливают объем воды в шприце по максимальной градуированной вместимости.
В.5. Перекрывают контрольную втулку.
В.6. Прикладывают боковое усилие на упор штока, направленное под прямым углом к нему, и раскачивают шток в радиальном направлении вокруг уплотнения поршня с силой, соответствующей значениям, указанным в табл.4. Шток необходимо отклонять максимально от его осевого положения.
Таблица 4
Номинальная вместимость шприца, см | Усилие, Н |
1 | 0,25 |
2 | 1,0 |
5 | 2,0 |
10 | 3,0 |
20 | 3,0 |
30 | 3,0 |
50 | 3,0 |
В.7. К шприцу прилагают такое осевое усилие, чтобы взаимодействующие поршень и цилиндр создали давление 300 кПа* для шприцев вместимостью менее 20 см и 200 кПа для шприцев вместимостью 20 см
и более. Выдерживают это давление в течение 30 с.
_________________
* 1 кПа=7,5 мм рт.ст.
В.8. Проверяют шприц на герметичность уплотнения поршня и герметичность соединения с контрольной втулкой.
ПРИЛОЖЕНИЕ С (обязательное). ИСПЫТАНИЕ НА ВОЗДУХОНЕПРОНИЦАЕМОСТЬ ПОРШНЯ И НАКОНЕЧНИКА ШПРИЦА ПРИ ВСАСЫВАНИИ
ПРИЛОЖЕНИЕ С
Обязательное
С.1. Испытание на воздухонепроницаемость поршня при всасывании
Испытание должно производиться с использованием аппарата, указанного на черт.3, следующим образом.
Черт.3. Аппарат для испытания на всасывание
Аппарат для испытания на всасывание
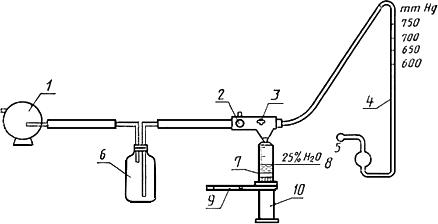
1 - вакуумный насос; 2 - регулятор малого истечения; 3 - вакуумный клапан; 4 - манометр*; 5 - насадка в соответствии с требованиями ИСО 594; 6 - ловушка; 7 - номинальный объем; 8 - 25%-ный объем воды; 9 - зажим; 10 - шприц
Черт.3
________________
* В СССР - вакуумметр.
С.1.1. В шприц набирают предварительно вскипяченную и охлажденную воду объемом не менее 25% градуированной вместимости.
С.1.2. Наконечник поднимают вверх, выдвигают шток так, чтобы линия отсчета совпала с отметкой максимальной вместимости, и зажимают шток в этом положении, как показано на черт.3.
С.1.3. Присоединяют наконечник шприца к контрольной стальной конической втулке в соответствии с требованиями ИСО 594.
С.1.4. Включают вакуумный насос при открытом регуляторе подачи воздуха.
С.1.5. Устанавливают регулятор так, чтобы происходило постепенное увеличение разрежения, доводя показание манометра до 88 кПа*.
_________________
* 1 кПа=7,5 мм рт.ст.
С.1.6. Проверяют шприц на воздухонепроницаемость уплотнения поршня.
С.1.7. Изолируют участок "шприц-манометр" через вакуумный клапан.
С.1.8. Следят за показаниями манометра в течение 60 с и записывают любое падение показаний манометра.
С.1.9. Проверяют шприц на разъединение поршня от штока.
С.2. Испытание на воздухонепроницаемость соединения наконечника и втулки при всасывании.
Испытания проводят следующим образом.
С.2.1. Соединяют наконечник шприца со стальной контрольной конической втулкой, причем обе части должны быть сухими. Контрольная втулка должна иметь внутреннюю 6%-ную конусность, соответствующую требованиям ИСО 594. Соединяют части, прикладывая осевое усилие 27,5 Н в течение 5 с, и поворачивают их на угол, не превышающий 90° с крутящим моментом не более 0,1 Н/м*.
________________
* См. приложение F.
С.2.2. Набирают в шприц предварительно вскипяченную и охлажденную воду, объемом не менее 25% градуированной вместимости шприца. Соединение гнезда с наконечником должно быть сухим.
С.2.3. Выпускают воздух, кроме небольшого количества воздушных пузырьков.
С.2.4. Устанавливают объем воды в шприце, равный 25% градуированной вместимости.
С.2.5. Перекрывают контрольную коническую втулку.
С.2.6. Наконечник шприца направляют вниз, выдвигают шток до номинальной градуированной вместимости и выдерживают его в таком положении в течение 15 с.
С.2.7. Проверяют шприц на образование непрерывных пузырьков из соединения наконечника шприца и стальной контрольной конической втулки. Пузырьки воздуха, образовавшиеся в течение первых 5 с, в расчет не принимают.
ПРИЛОЖЕНИЕ D (обязательное). ОПРЕДЕЛЕНИЕ ОБЪЕМА "МЕРТВОГО" ПРОСТРАНСТВА
ПРИЛОЖЕНИЕ D
Обязательное
D.1. Методика определения
D.1.1. Взвешивают пустой шприц.
D.1.2. Заполняют шприц дистиллированной водой до полной градуированной вместимости, удаляя все пузырьки воздуха, при этом уровень мениска воды должен совпадать с концом отверстия наконечника.
D.1.3. Вытесняют воду, полностью опустив шприцевой поршень, и вытирают насухо наружную поверхность.
D.1.4. Шприц взвешивают снова.
D.2. Подсчет результатов
Определяют массу воды, оставшуюся в шприце, в граммах путем вычитания массы пустого шприца из массы шприца после вытеснения из него воды. Записывают объем "мертвого" пространства в кубических сантиметрах, принимая во внимание, что плотность воды равняется единице.
ПРИЛОЖЕНИЕ Е (рекомендуемое). РЕКОМЕНДУЕМЫЙ МЕТОД ПРОВЕРКИ НЕСОВМЕСТИМОСТИ ШПРИЦЕВ И ИНЪЕКЦИОННЫХ ЖИДКОСТЕЙ
________________
* См. приложение F.
Е.1. Введение
Выбор растворителей и других жидкостей, используемых для приготовления вводимых инъекционных препаратов, подходящий для проверки шприца на совместимость, приводится ниже. Этот перечень материалов рекомендуется в качестве готовых средств, указывающих на совместимость шприцев и веществ, использующихся во вводимых инъекционных препаратах. Этот метод испытания дается лишь в качестве рекомендации.
Е.2. Список растворителей и других жидкостей, используемых в инъекционных жидкостях:
вода;
этанол+вода (5% об.);
1,2-пропандиол+вода (10% об.);
фракционированное кокосовое масло;
арахисовое масло;
арахисовое масло+бензиловый спирт (10% об.);
арахисовое масло+бензилбензоат (10% об.);
этилолеат;
иодированное масло (масло семян мака с 37-39% иода);
иофендиалат;
паральдегид.
Е.3. Испытание для определения видимой и функциональной несовместимости шприцев и инъекционных жидкостей.
Наполняют два шприца испытуемой жидкостью, переворачивают их и выдерживают при температуре 20 °C. Через 2 ч 10 мин удаляют жидкость из шприца. При этом не должно быть приложения больших усилий, чем необходимо для передвижения штока. Протирают все поверхности бумажной салфеткой и проверяют, нет ли каких-либо изменений во внешнем виде, появления помутнения или окраски на шприце или выпущенной жидкости. Признаком несовместимости может служить разбухание каучука и (или) трещины, разъедание, прилипание или размягчение внутренней поверхности пластмассового цилиндра шприца.
ПРИЛОЖЕНИЕ F (обязательное). ДОПОЛНИТЕЛЬНЫЕ ТРЕБОВАНИЯ, ОТРАЖАЮЩИЕ ПОТРЕБНОСТИ НАРОДНОГО ХОЗЯЙСТВА СССР
ПРИЛОЖЕНИЕ F
Обязательное
F.1. Назначение и область применения. Настоящий стандарт распространяется на инъекционные шприцы однократного применения (далее - шприцы), используемые в медицинской практике для подкожного внутримышечного и внутривенного введения в организм лекарственных средств, а также для отсасывания различных жидкостей из организма.
Стандарт не распространяется на инъекционные шприцы однократного применения, поставляемые наполненными лекарствами, и инсулиновые шприцы.
Шприцы изготовляют в климатическом исполнении УХЛ4.2 по ГОСТ 15150.
Примечание. Приведенные в приложении F пп.F.1; F.4; F.14.3; F.20.1; F.20.2; F.E действуют совместно с основным текстом стандарта, пп.F.6; F.7; F.9.1; F.13.4; F.19; F.A.1; F.B; F.C.2.1;
введены взамен соответствующих пунктов стандарта.
F.4. Материалы. F.4.1. Материалы, из которых должны быть изготовлены детали шприцев и потребительская тара, должны быть разрешены компетентными органами здравоохранения.
F.6. Отсутствие пирогенных веществ. Шприцы должны удовлетворять требованиям настоящего стандарта при испытаниях на отсутствие пирогенных веществ.
Испытания шприцев на пирогенность должны проводить в соответствии с "Регламентом проведения санитарно-химических, токсикологических и биологических испытаний стерилизованных шприцев инъекционных однократного применения", утвержденным Минздравом СССР.
Экстракт, используемый для этого испытания, должен готовиться с соблюдением методики, указанной в п.А.2.
F.7. Испытание на сверхдопустимое содержание токсичных веществ. Шприцы должны удовлетворять требованиям настоящего стандарта в части испытаний на сверхдопустимое содержание токсичных веществ.
Испытания шприцев на токсичность должны проводиться в соответствии с "Регламентом проведения санитарно-химических, токсикологических и биологических испытаний стерилизованных шприцев инъекционных однократного применения", утвержденным Минздравом СССР.
Экстракт, используемый в этом испытании, должен готовиться по методу, указанному в п.А.2.
F.9. Требования, предъявляемые к экстрагируемому веществу. F.9.1. Общие положения
Шприц должен удовлетворять требованиям химических испытаний на экстрагируемое вещество в соответствии с "Регламентом проведения санитарно-химических, токсикологических и биологических испытаний стерилизованных шприцев инъекционных однократного применения", утвержденным Минздравом СССР.
F.13. Градуированная шкала. F.13.4. Расположение шкалы
При нахождении штока в крайнем положении, когда он до упора смещен к отверстию наконечника цилиндра, нулевая отметка шкалы должна совпадать с линией начального отсчета на поршне (п.15.3) в пределах четверти наименьшего деления шкалы.
У шприцев шкала должна находиться между упорами для пальцев.
F.14. Цилиндр. F.14.3. Упор для поршня
Цилиндр шприца должен иметь упор, препятствующий самопроизвольному выпадению штока-поршня из цилиндра при вертикальном положении шприца.
F.19. Стерильность. Шприцы в ненарушенных упаковках (п.18.1) должны быть стерильными.
Проверку стерильности шприцев проводят согласно "Методике контроля стерильности шприцев инъекционных однократного применения, простерилизованных газовым методом", утвержденной 25.08.89 или "Методическими указаниями по контролю стерильности медицинских изделий, стерилизованных радиационным способом" (приложением к Приказу N 964/410 от 17.09.79 Минздрава СССР и Минмедпрома).
F.20. Маркировка упаковки. F.20.1. Потребительская упаковка
б) слова: "СТЕРИЛЬНО"; "АПИРОГЕННО";
ж) слова: "Годен до..." (месяц и две последние цифры года).
F.20.2. Внешняя упаковка
б) слова: "СТЕРИЛЬНО"; "АПИРОГЕННО"; "НЕТОКСИЧНО";
д) номер партии или дата (месяц и год) стерилизации;
е) наименование и (или) товарный знак предприятия-изготовителя;
ж) количество шприцев;
з) слова: "Годен до..." (месяц и две последние цифры года).
F.A. Приготовление экстрактов. F.A.1. Методика приготовления
При приготовлении экстрактов используют режим с температурой 40 °С и временем 24 ч и емкость из стекла в соответствии с "Регламентом проведения санитарно-химических, токсикологических и биологических испытаний стерилизованных шприцев инъекционных однократного применения", утвержденным Минздравом СССР.
F.B. Проверка водонепроницаемости уплотнения штока-поршня в цилиндре и конусного соединения цилиндра с головкой инъекционной иглы. F.B.1. Соединяют наконечник шприца со стальной контрольной втулкой (обе части должны быть сухими). Контрольная втулка должна иметь внутреннюю 6%-ную конусность Луер в соответствии с требованиями ИСО 594. Соединяют наконечник шприца с контрольной втулкой, поворачивая их на угол, не превышающий 90°.
F.B.2. Набирают в шприц воду, объем которой превышает градуированную вместимость шприца. Соединение втулки с наконечником должно быть сухим.
F.B.3. Выпускают воздух
F.B.4. Устанавливают объем воды в шприце по максимальной градуированной вместимости.
F.B.5. Перекрывают контрольную втулку.
F.B.6. К штоку-поршню шприца прилагают такое осевое усилие, чтобы взаимодействующий поршень и цилиндр создавали давление 300 кПа - для шприцев вместимостью менее 20 см и 200 кПа - для шприцев вместимостью 20 см
и более. Выдерживают это давление в течение 30 с.
F.B.7. Проверяют шприц на герметичность уплотнения поршня и герметичность соединения с контрольной втулкой.
F.B.8. Допускается проверку водонепроницаемости для трехдетальных шприцев проводить следующим образом.
Испытания проводят на установке, собранной по схеме, указанной на черт.4.
Черт.4. Схема установки для испытания шприцев на водонепроницаемость
Схема установки для испытания шприцев на водонепроницаемость
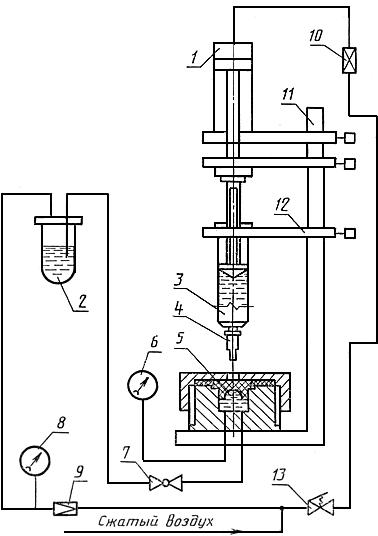
1 - цилиндр пневматический; 2 - сосуд с окрашенной водой; 3 - шприц однократного применения; 4 - игла однократного применения; 5 - напорная камера; 6 - манометр; 7 - проходной кран; 8 - манометр; 9 - редукционный клапан; 10 - дроссельный клапан; 11 - штатив; 12 - упорные пластины; 13 - самозапорный клапан
Черт.4
Подготовка к испытаниям:
вращением крана 9 регулируют давление воздуха до 0,3 МПа (3 кгс/см)*, измеряемое манометром 8;
________________
* Текст соответствует оригиналу. - Примечание изготовителя базы данных.
заливают в сосуд 2 окрашенную воду с температурой (20+5) °С; **
________________
* Текст соответствует оригиналу. - Примечание изготовителя базы данных.
на шприц одевают иглу однократного применения;
устанавливают шприц с иглой в напорную камеру 5 и регулируют положение упорных пластин;
включением крана 7 заполняют шприц водой до номинальной вместимости;
вращая винт клапана 10 и включая клапан 13, регулируют количество поступающего в цилиндр 1 воздуха в объеме, обеспечивающем опорожнение шприца в течение не более 30 с.
Испытания необходимо проводить в следующей последовательности:
с применением динамометра одевают на шприц иглу с усилием (27,5±1,0) Н;
вставляют шприц с иглой в напорную камеру 5;
заполняют шприц водой до номинальной вместимости;
извлекают шприц с иглой из напорной камеры 5 и вручную удаляют воздух;
вновь вставляют шприц с иглой в напорную камеру 5 и заполняют водой;
удаляют воду из шприца, контролируя манометром 6, при этом противодавление воды (0,30±0,01) МПа [(3,0±0,1) кгс/см] - для шприцев вместимостью 1, 2, 5 и 10 см
и (0,20±0,01) МПа [(2,0±0,1) кгс/см
] - для шприцев вместимостью 20 см
;
визуально осматривают шприц. Шприц считается годным, если над уплотнительным элементом штока-поршня не будет обнаружена вода. Допускается в месте соединения наконечника шприца с головкой иглы появление капли воды, которая не должна падать за время менее 10 с.
F.C. Проверка воздухонепроницаемости уплотнения штока-поршня в цилиндре и конусного соединения цилиндра с головкой инъекционной иглы. F.C.2.1. Соединяют наконечник шприца со стальной контрольной конической втулкой, причем обе части должны быть сухими. Контрольная втулка должна иметь внутреннюю 6%-ную конусность Луер, соответствующую требованиям ИСО 594. Соединяют наконечник шприца с контрольной втулкой, поворачивая их на угол, не превышающий 90°.
F.E. Рекомендуемые список фармакопейных препаратов и растворов, применяемых в СССР для инъекций и удовлетворяющих требованию совместимости со шприцами, и метод их проверки. F.E.1. Список препаратов и растворов
Вода дистиллированная.
Спирт этиловый 95%-ный.
Спирт этиловый 33%-ный.
Масло абрикосовое.
Раствор камфоры в абрикосовом масле 20%-ный.
Раствор глюкозы 40%-ный.
Раствор хлористого натрия 0,9%-ный.
Раствор магния сульфата 20%-ный.
Раствор кальция хлорида 10%-ный.
Раствор эуфиллина 12%-ный.
Раствор натрия тиосульфата (гипосульфита) 30%-ного + 2%-ного натрия гидрокарбоната.
F.E.2. Метод проверки
Проверку совместимости материалов шприцев с лекарствами проводят органы здравоохранения с 01.01.94 по следующей методике.
Наполняют два шприца лекарством, переворачивают их и выдерживают при температуре (20±5) °С для водных и спиртовых растворов, при температуре (40±5) °С - для масляных растворов. Через 2 ч 10 мин удаляют жидкость из шприца. При этом не должно быть приложения больших усилий, чем необходимо, для передвижения штока. Протирают все поверхности бумажной салфеткой и проверяют, нет ли каких-либо изменений во внешнем виде, появления помутнения или окраски на шприце или выпущенной жидкости. Признаком несовместимости может служить вспучивание резиновой манжеты, трещины, разъедание, прилипание или размягчение внутренней поверхности цилиндра шприца.